起动电池和深循环电池的结构差异
是什么使得一个电池可以在短时间内提供高突发电流,而另一个电池可以在较长时间内提供低电流?
答案在于引线板的厚度。
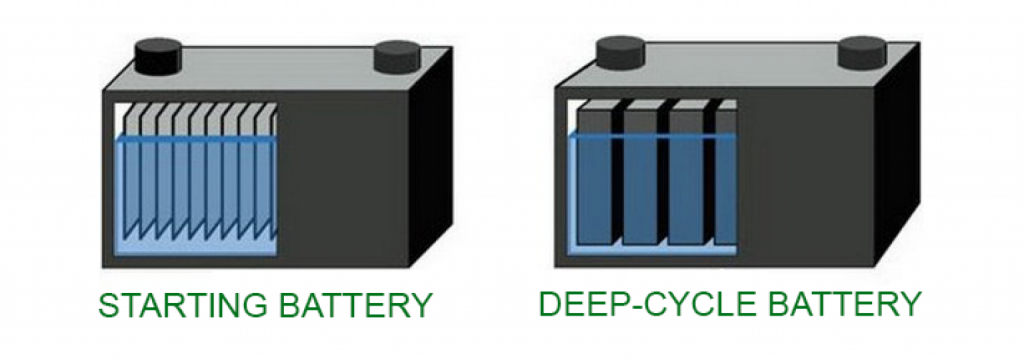 深循环电池具有更厚的铅板,可以承受更大的放电深度。
深循环电池具有更厚的铅板,可以承受更大的放电深度。深循环电池的铅板比起动电池厚得多。这种极板厚度的差异使得深循环电池中的极板更加坚固并且不太可能弯曲。
因此,它们在长时间传输电流时不会立即受到损坏。
铅是一种软金属,因此如果您使用启动电池作为深循环电池,薄铅板很可能会开始弯曲/变形。这会影响电池的性能并最终缩短其使用寿命。
使深循环电池更能抵抗大深度放电的另一个因素是铅板之间的隔板类型。
为了提高耐用性和提高性能,设计了两种类型的铅酸电池(AGM 和凝胶)。
在本文中,我们将讨论用于深循环目的的 AGM 电池与凝胶电池。
铅酸电池:AGM 与。凝胶
要了解AGM电池与凝胶电池的不同之处,您首先需要了解铅酸电池的工作原理,因为这种化学原理适用于 AGM 和凝胶电池。
电池内部有多个电池单元(电池单元的数量决定了电池的电压)。12V铅酸电池有6节电池串联。
铅酸电池的主要部件
在每个单元格中,您会发现:
铅板(正极,PbO 2 (s) 和负极,Pb(s))
这些板之间有一个隔板
促进氧化还原反应的电解质
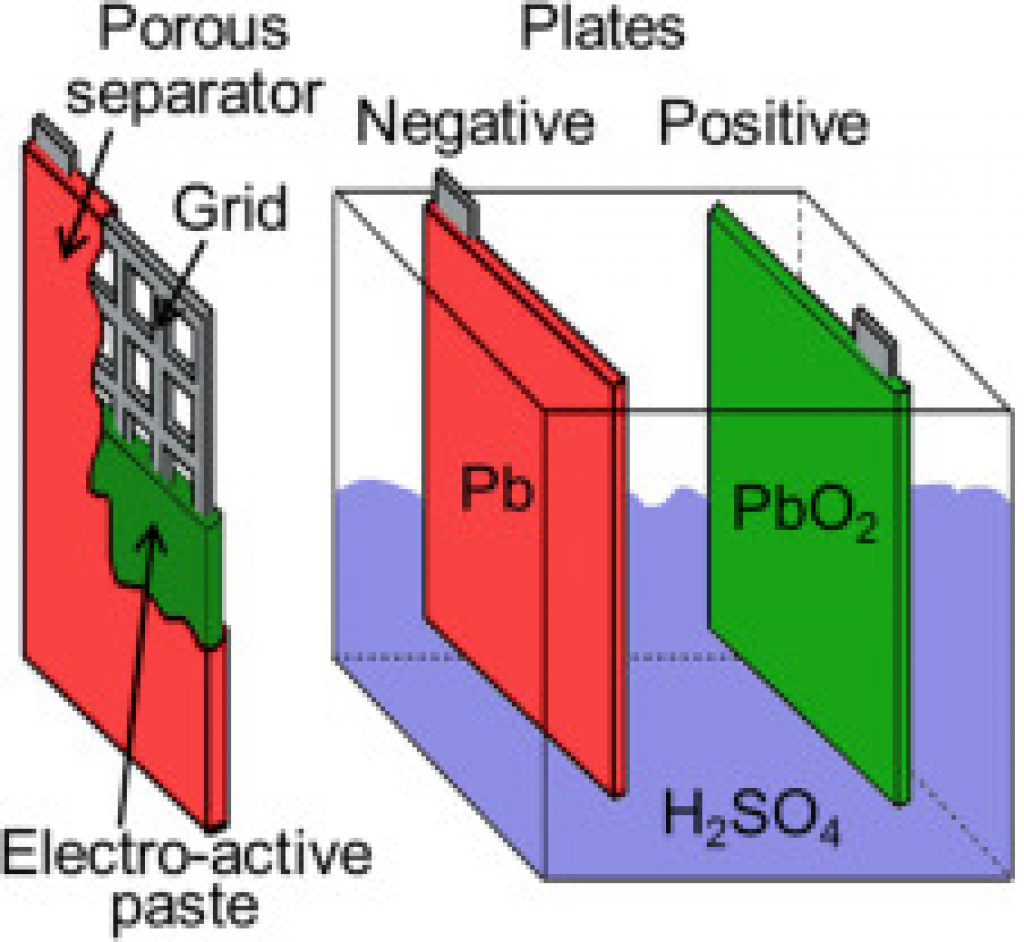 铅酸电池的图示。
铅酸电池的图示。铅板形状为网格以增加表面积。此外,在极板周围涂有电活性膏。
用作隔膜的材料取决于铅酸电池的类型。在 AGM 电池中,隔膜是玻璃垫。在凝胶电池中,将二氧化硅添加到电解质中以形成充当隔膜的凝胶。
电解质是硫酸(H 2 SO 4 )溶液。
化学反应
现在您已经了解了铅酸电池的主要成分,让我们更深入地了解它们的电化学。
与所有可充电电池一样,铅酸电池具有发生可逆化学反应的电化学电池。
当电池充电时,电能转化为化学能,相反,放电时,化学能转化为电能。
这些转化能量的反应是什么?
铅酸电池的正极板是二氧化铅(PbO 2 ),负极板是铅(Pb)。
这些极板分离并与电解质发生反应(参与还原和氧化反应)。
电解质是硫酸(H 2 SO 4 )的水溶液。
当铅酸电池充满电时,硫酸溶液处于最高浓度:
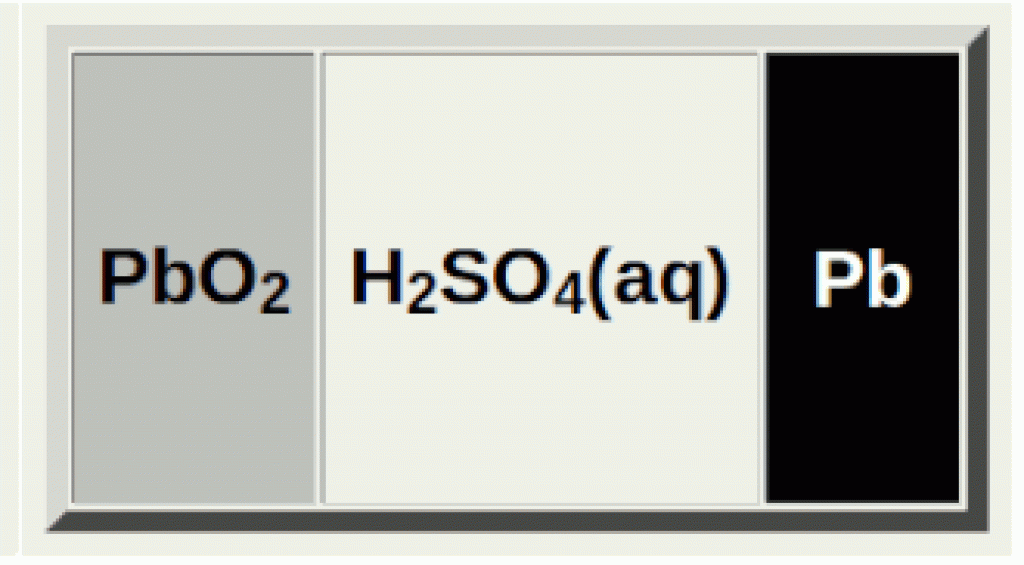 充满电的铅酸电池:
充满电的铅酸电池:Pb(s)、PbO 2 (s) 和 H 2 SO 4 (aq)
一旦将电池连接到负载,就会自发放电。“负极”板在放电过程中遭受氧化 - Pb 与电解质反应形成 PbSO 4(在此过程中释放电子)。
半反应:Pb(s) + HSO − 4 (aq) → PbSO 4 (s) + H + (aq) + 2e −
同时,“正极”板发生还原:PbO 2与酸反应形成PbSO 4 (s) 和水。
半反应:PbO 2 (s) + HSO − 4 (aq) + 3H + (aq) + 2e − → PbSO 4 (s) + 2H 2 O(l)
这个过程将存储在电池中的化学能转化为电能,为设备提供动力。
一旦电池完全放电,电解质就处于最低浓度(非常稀释),并且两个电极主要是 PbSO 4。
 完全放电的铅酸电池:
完全放电的铅酸电池:PbSO 4 (s) 和稀释的 H 2 SO 4 (aq)
当您向电池施加外部电源时,会发生相反的反应,将电能转化为化学能。这样,电池就可以执行多次循环。
总反应:Pb(s) + PbO 2 (s) + 2H 2 SO 4 (aq) → 2PbSO 4 (s) + 2H 2 O(l)
该电化学电池的电位差为+2.05V。这就是为什么 12V 电池有 6 个串联电池,因为 6 x 2.05V = 12.3V(12V 铅酸电池的标称电压)。
起动电池和深循环电池的结构差异
是什么使得一个电池可以在短时间内提供高突发电流,而另一个电池可以在较长时间内提供低电流?
答案在于引线板的厚度。
 深循环电池具有更厚的铅板,可以承受更大的放电深度。
深循环电池具有更厚的铅板,可以承受更大的放电深度。深循环电池的铅板比起动电池厚得多。这种极板厚度的差异使得深循环电池中的极板更加坚固并且不太可能弯曲。
因此,它们在长时间传输电流时不会立即受到损坏。
铅是一种软金属,因此如果您使用启动电池作为深循环电池,薄铅板很可能会开始弯曲/变形。这会影响电池的性能并最终缩短其使用寿命。
使深循环电池更能抵抗大深度放电的另一个因素是铅板之间的隔板类型。
为了提高耐用性和提高性能,设计了两种类型的铅酸电池(AGM 和凝胶)。
在本文中,我们将讨论用于深循环目的的 AGM 电池与凝胶电池。
铅酸电池:AGM 与。凝胶
要了解AGM电池与凝胶电池的不同之处,您首先需要了解铅酸电池的工作原理,因为这种化学原理适用于 AGM 和凝胶电池。
电池内部有多个电池单元(电池单元的数量决定了电池的电压)。12V铅酸电池有6节电池串联。
铅酸电池的主要部件
在每个单元格中,您会发现:
铅板(正极,PbO 2 (s) 和负极,Pb(s))
这些板之间有一个隔板
促进氧化还原反应的电解质
 铅酸电池的图示。
铅酸电池的图示。铅板形状为网格以增加表面积。此外,在极板周围涂有电活性膏。
用作隔膜的材料取决于铅酸电池的类型。在 AGM 电池中,隔膜是玻璃垫。在凝胶电池中,将二氧化硅添加到电解质中以形成充当隔膜的凝胶。
电解质是硫酸(H 2 SO 4 )溶液。
化学反应
现在您已经了解了铅酸电池的主要成分,让我们更深入地了解它们的电化学。
与所有可充电电池一样,铅酸电池具有发生可逆化学反应的电化学电池。
当电池充电时,电能转化为化学能,相反,放电时,化学能转化为电能。
这些转化能量的反应是什么?
铅酸电池的正极板是二氧化铅(PbO 2 ),负极板是铅(Pb)。
这些极板分离并与电解质发生反应(参与还原和氧化反应)。
电解质是硫酸(H 2 SO 4 )的水溶液。
当铅酸电池充满电时,硫酸溶液处于最高浓度:
 充满电的铅酸电池:
充满电的铅酸电池:Pb(s)、PbO 2 (s) 和 H 2 SO 4 (aq)
一旦将电池连接到负载,就会自发放电。“负极”板在放电过程中遭受氧化 - Pb 与电解质反应形成 PbSO 4(在此过程中释放电子)。
半反应:Pb(s) + HSO − 4 (aq) → PbSO 4 (s) + H + (aq) + 2e −
同时,“正极”板发生还原:PbO 2与酸反应形成PbSO 4 (s) 和水。
半反应:PbO 2 (s) + HSO − 4 (aq) + 3H + (aq) + 2e − → PbSO 4 (s) + 2H 2 O(l)
这个过程将存储在电池中的化学能转化为电能,为设备提供动力。
一旦电池完全放电,电解质就处于最低浓度(非常稀释),并且两个电极主要是 PbSO 4。
 完全放电的铅酸电池:
完全放电的铅酸电池:PbSO 4 (s) 和稀释的 H 2 SO 4 (aq)
当您向电池施加外部电源时,会发生相反的反应,将电能转化为化学能。这样,电池就可以执行多次循环。
总反应:Pb(s) + PbO 2 (s) + 2H 2 SO 4 (aq) → 2PbSO 4 (s) + 2H 2 O(l)
该电化学电池的电位差为+2.05V。这就是为什么 12V 电池有 6 个串联电池,因为 6 x 2.05V = 12.3V(12V 铅酸电池的标称电压)。







